タダラフィルは血管拡張作用を持つカルボリンをベースとする化合物です。
タダラフィルは、環状2,5-ジケトピペラジンであり、1,2,3,4-テトラヒドロ-β-カルボリンでもあります。

タダラフィルは、ホスホジエステラーゼ5(PDE5)阻害剤と呼ばれる医薬品のグループに属しており、勃起不全(ED)、良性前立腺過形成(BPH)、および肺動脈高血圧(PHA)の治療に使用される薬剤です。新薬は経口投薬の錠剤タイプで提供されており、作用があらわれ始める時間は通常30分以内で、持続時間は最大36時間まで続きます。
化学名
(6R,12aR)-6-(1,3-Benzodioxol-5-yl)-2-methyl-2,3,6,7,12,12a-hexahydropyrazino[1′,2′:1,6]pyrido[3,4-b]indole-1,4-dione
分子式 C22H19N3O4
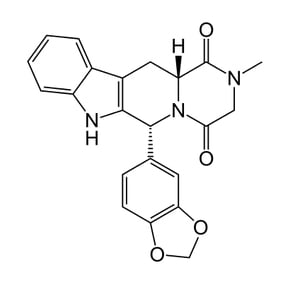
タダラフィルは血管拡張作用を持つカルボリンをベースとする化合物です。
タダラフィルは、環状2,5-ジケトピペラジンであり、1,2,3,4-テトラヒドロ-β-カルボリンでもあります。

有効成分タダラフィルは、主に男性のED(勃起不全)の治療に使用される経口投与薬です。性交が終わる際に勃起を萎えさせるために放出される酵素であるホスホジエステラーゼ5(PDE5)を阻害します。ED(勃起不全)を患っている男性の体内では PDE5が性交の最中に早く放出されるため、PDE5を阻害することで症状を防ぎます。ペニスは、PDE5が放出される領域の1つになります。PDE5を阻害するとペニスのGMPの濃度が上昇するので、海綿体の平滑筋が弛緩し血管拡張をもたらし、勃起をサポートします。
タダラフィル錠は「シアリス(Cialis)」というブランド名で2003年から国際的に販売されはじめました。日本では2007年より5mg, 10mg, 20mgの用量が承認され、販売されています。
ED(勃起不全)とは、男性が性的に興奮している際に、勃起を維持することができない、またはペニスの硬さが不足したり中折れしたりする症状を指します。重症の場合は全く勃起を得ることができなくなります。
世界的に見て3000万人もの男性がEDを患っていると報告されています。また、日本人男性の4人の1人はED、50〜60代になると2人に1人はEDだと報告されています。一般的にEDは、糖尿病、心臓病、高血圧などの心血管疾患と生活習慣病などの病気と共通の病因を持っており、その有病率は年齢とともに増加する傾向があります。
同じPDE5阻害薬の医薬品のグループに属するお薬として有効成分シルデナフィル(商品名:バイアグラ)、バルデナフィル(商品名:レビトラ)、アバナフィル(商品名:ステンドラ)などがあります。これらのお薬は主にED(勃起不全)を治療するために使用されています。PDE5阻害薬は、高齢の患者を含むほとんどの男性にとって安全に有効性をもたらすことができることから、医師が選ぶ第一選択肢となる治療法でもあります。お薬の作用による有効性は、女性の膣への挿入に十分な勃起を得ることと定義され、このことは満足の行く快感を与える性交の成功にも繋がります。
タダラフィルの最も際立った薬理学的特徴は、有効成分シルデナフィル(商品名:バイアグラ)の4〜5時間と有効成分バルデナフィル(商品名:レビトラ)の4〜8時間の半減期と比較すると、特出して長い半減期(17.5時間)にあります。半減期とは、お薬を服用してから効果が半減するまでの時間であり、より長い半減期はより長い効果持続時間をもたらします。
タダラフィル(商品名:シアリス)は水に溶けにくい性質を有しています。この性質が長い効果持続時間を与えることを可能にします。シアリスは1錠を服用することで最大で36時間まで効果が続くため、「ウィークエンドピル」と呼ばれ親しまれています。
タダラフィルを毎日同じ時間帯に低用量(2.5mgまたは5mg)で服用することで、服用のタイミングを気にせずにいつでも好きな時に性交することができる用法があります。「シアリス・デイリー」は、PDE5阻害薬の中で初めて男性に長期的な治療を提供しました。タダラフィルは、服用方法の柔軟性と薬理作用の長い効果持続時間をもたらすことで、性交への心理的プレッシャーを取り除き、また陰茎の勃起につながる生理学的機能の両方を改善することができる画期的なお薬です。タダラフィルは、必要な時に服用する単発治療だけでなく長期治療においても、ED治療の有効性と安全性が確認された初めてのお薬です。
シアリス・デイリーは2008年1月にFDAより承認されました。日本では2019年現在厚生労働省からの承認はされていません。
性的刺激を受けた男性の身体では一酸化窒素(NO)が局所的に陰茎組織で放出されます。一酸化窒素は平滑筋細胞における環状グアノシン一リン酸(GMP)を産出し、このGMPが平滑筋の弛緩を引き起こし陰茎の血管が拡張します。この作用により海綿体への血流が増加し、勃起が引き起こされます。
ホスホジエステラーゼ5型(PDE5)阻害薬はPDE5を阻害し、GMPの量を増やすことで勃起の機能を高めます。
ただし、性的刺激が一酸化窒素(NO)の局所陰茎放出を誘発するため、PDE5阻害を服用しても、性的刺激がないと効果がありません。
2003年に発刊された医学誌 Journal of Sexual and Reproductive Medicineに掲載されたジェラルド・ブロック(Gerald Brock)医師による研究報告によると、5件の無作為化二重盲検プラセボ対照多施設試験(その内、カナダの患者を対象とした試験は4件)は、2.5mg、5mg、10mg、20mgの用量のタダラフィルを研究しました。
統合分析において、タダラフィルはプラセボと比較して、すべての有効性の結果で統計的に有意な改善を示しました。国際勃起機能スコアの質問では、タダラフィル20 mgを服用した男性の81%が勃起の全体的な改善を報告しました。
別の研究において、タダラフィルは投与後36時間にわたり勃起機能を著しく改善しました。タダラフィルは一般的に他のPDE5阻害剤と比較して副作用がでにくく、良好な効果をもたらすことがわかっています。
シアリスの効果についてより詳しい情報を知りたい方はこちらをクリックして シアリスの効果の記事をご参照ください。
タダラフィルは、良性前立腺肥大症(BPH)の徴候や症状がある男性の治療にも使用されます。
前立腺肥大症は、男性が加齢すると共に前立腺が肥大してしまうことが原因で、尿道で抵抗が増大し引き起こされる症状です。 BPHの男性は通常、排尿障害、排尿の減少、排尿開始時の困難などの症状が生じ、夜間に起きて排尿する必要性が生じます。
アテローム性動脈硬化症が生じると、尿路周辺の下部組織への血流にも影響し、前立肥大症にかかりやすくなるとされています。
タダラフィルは、これらの症状を緩和し、前立腺手術が必要になる可能性を減らします。日本では「ザルティア(Zalutia)」というという商品名で2014年4月より販売されています。用量は5mgまたは2.5mgの錠剤タイプのお薬です。
タダラフィルは下部尿路組織と血管内のPDE5を阻害することで、cGMP濃度を上昇させ、その結果、血管の平滑筋が弛緩し、血流と酸素供給量が増加します。タダラフィルは前立腺、尿道、膀胱周辺部の平滑筋も弛緩させる作用をもたらし、排尿障害を改善させるサポートを行います。
The Journal of Urology、Volume 180、Issue 4(October 2008)に掲載されている論文「良性前立腺過形成にともなう下部尿路症改善のためにタダラフィルを1日1回投与することについて:用量設定試験」によると、良性前立腺過肥大症(BPH)を患う男性が、タダラフィル(シアリス)を毎日服用することで、下部尿路症状(LUTS)を軽減することができたことが報告されています。
研究の参加者は、良性前立腺過肥大症BPHにともなう下部尿路症状(LUTS)を少なくとも6ヶ月以上患っている病歴を有することが必要とされました。
PSAが10 ng / mlを超え高い被験者は除外され、他の複雑な病状や薬物治療の相互作用がある被験者も除外されました。
参加者はまず、4週間の治療を行わないスクリーニング期間を受けました。
その後、すべての参加者は、無作為で4週間前にプラセボを投与されました。次に、1056人の被験者を無作為に5つのグループに分け、プラセボまたはタダラフィルが1日あたり2.5mg、5 mg、10 mg、20mg投与されました。
国際前立腺症スコア(I-PSS)を使用した、最後の月にあらわれた下部尿路症に関する7項目のアンケートの結果、タダラフィルのすべての用量において、下部尿路症を軽減するための効果が、プラセボよりも優れていることが報告されました。
12週間の治療後、異なる用量のグループにおいてI-PSSスコアが3.9ポイント〜5.2ポイントの間で減少し、改善したことが報告されました。これは、米国泌尿器科学会のガイドラインに従って臨床的に有意義な改善とみなすことができる数値ということになります。研究で使用された用量のうち、1日5 mgのタダラフィルがI-PSSを4.9ポイント改善し、最高のリスク-ベネフィット(risk-benefit)指数を記録しました。
タダラフィルは男性と女性の肺動脈高血圧症(PHA)の症状を治療し、運動能力を向上させるためにも使用されます。
肺動脈高血圧症(PHA)とは、心臓から肺に血液を運ぶ肺動脈で発生する高血圧の症状です。何らかの原因により、肺動脈の血管が厚くなったり狭くなったり収縮することで血管が狭くなることが原因だと考えられています。
肺の抹消血管が血流に対してより抵抗力を持つようになると、肺を通して十分な血液を送り出すために右心室がより激しく働かなければならず、心臓への負担が大きくなります。心臓の右側からより強い圧力をかけて肺へ血液を送りつづけると、心臓の右心の筋肉がやがて肥大するようになり、全身に酸素を運ぶ血液を送り出すポンプとしての機能が低下し、しだいに全身の機能が低下していきます。
タダラフィルは肺動脈のPDE5を阻害し、cGMPレベルを上昇させ血管を弛緩させます。これにより、肺への血液の供給が増加し、心臓の負担が軽減されます。
タダラフィルの長い半減期は、肺動脈高血圧症における1日1回療法としての使用を可能にさせました。
PAHの治療に推奨されるタダラフィルの用量は1日1回40 mgです。20 mgの錠剤を2つ服用します。医師は1日1錠から投与を開始し、1日2錠に用量を増やして調整することができます。
肺動脈高血圧症(PHA)へのタダラフィルは「アドシルカ(Adcirca)」という商品名で2009年12月より日本での販売が開始されました。
タダラフィルが全身の血管(動脈)を弛緩させるため、全身の血圧が低下する場合があります。たとえば、90/50 mmHg未満の低血圧の患者は、服用の際に注意が必要です。脱水症状、左心疾患、身体の神経系機能に特定の持病を患っている患者も注意が必要です。
タダラフィルはPDE5阻害薬という医薬品のグループに属します。
ホスホジエステラーゼ5(PDE5)は、肺や陰茎など身体のいくつかの部分で生成される酵素である環状グアノシン一リン酸(GMP)と呼ばれる化学物質を分解します。GMPは主に血管(動脈)を弛緩させる拡張作用をもたらします。
タダラフィルはPDE5を阻害するため、肺内の血管でよりGMPが活性し、血管の弛緩と拡張作用をもたらします。肺の血管の弛緩と拡張は、心臓への肺血圧を低下させ、心血管機能を改善します。この作用により、肺の血圧が低下し、より活動的に肺機能の改善をサポートします。
16週間の二重盲検プラセボ対照試験において、405人の肺動脈高血圧症の患者が、治療未経験、またはエンドセリン受容体拮抗薬ボセンタンによる療法を受けたことが有るかのいずれかで、プラセボまたはタダラフィルに無作為に分けられ投与されました。
2.5mg、10mg、20 mg、または40 mgが1日1回経口投与されました。
主要の評価の基準は、6分間の歩行における距離の長さが、服用前の研究初期から16週目までにどれ程変化したかということでした。
世界保健機関が定めた機能分類の変化、臨床的に悪化したかどうか、健康関連の生活の質も評価されました。
16週間の研究を終了した患者は、長期研究に参加することができます。
その結果、タダラフィルは6分間に歩行した距離を、用量ごと違いはありましたが、増加させました。
40 mgの用量のみが、事前に指定された統計的有意性のレベルを満たしたレベルで増加させました。
全体の統計をみると、プラセボのグループは平均で33 mでした。
ボセンタン未投与群では平均で44 mでした。
ボセンタン療法を受けたことのある患者では23 mでした。
タダラフィル40 mgは、臨床的悪化までの期間、臨床的悪化の発生率、および健康関連の生活の質の全てを改善させました。
世界保健機関の機能分類の変化は統計的に有意ではありませんでした。
タダラフィルで報告された最も一般的な副作用は、頭痛、筋肉痛、ほてりでした。
結論として、肺動脈高血圧症の患者においては、タダラフィル40 mgの忍容性が最も高いことが確認され、患者の運動能力と生活の質の測定値が改善され、臨床的悪化が軽減されたことがわかりました。

タダラフィルは、主に肝臓のシトクロムP450 3A4 (CYP3A4)酵素システムによって代謝されます。
したがって、CYP3A4誘導剤はタダラフィルの半減期を短縮し、薬物の血清レベル、すなわち有効性を低下させる可能性があります。
一方CYP3A4遮断薬は、タダラフィルが体内で吸収されやすくなり、体内により長く残ってしまう作用をもたらします。成分が適量以上に作用して副作用が強く出たりすることに繋がります。
タダラフィル(商品名:シアリス)、シルデナフィル(商品名:バイアグラ)、バルデナフィル(商品名:レビトラ)はすべてホスホジエステラーゼ5(PDE5)の酵素を阻害することにより作用しますが、これらのお薬は他の種類の酵素であるPDE6、PDE 1、PDE 11もそれぞれ異なったレベルで阻害します。
シルデナフィルとバルデナフィルは、タダラフィルよりもホスホジエステラーゼ6(PDE6)をより多く阻害します。PDE6は目の網膜に最も多く見られる酵素です。シルデナフィルを服用した一部の男性の中には、青みがかった色に視覚が変化する副作用を経験したと報告されていますが、この副作用はPDE6阻害により光に対する感度が高くなっていることが原因だと考えられています。
シルデナフィルとバルデナフィルは、タダラフィルよりもホスホジエステラーゼ1(PDE1)をより多く阻害します。PDE1は脳、心臓、および血管の平滑筋に見られます。シルデナフィルとバルデナフィルによるPDE1の阻害はほてり、頻脈、血管拡張などの副作用の発症に繋がっていると考えられています。
タダラフィルは、シルデナフィルまたはバルデナフィルよりもホスホジエステラーゼ11(PDE11)をより多く阻害します。PDE11は骨格筋、前立腺、肝臓、腎臓、下垂体、および精巣に見られる酵素です。PDE11を阻害することによる身体への影響ははっきりと解明されていませんが、シアリス特有の副作用である四肢痛、背部痛、筋痛などの発症に影響していると考えられます。
タダラフィルを使用する場合の最も一般的な副作用は、頭痛、胃の不快感・痛み、消化不良、げっぷ、酸逆流性疾患、背中の痛み、筋肉痛、ほてり、鼻づまりです。
これらの副作用は、タダラフィルの血管拡張をもたらすPDE5阻害作用から引き起こされており、通常は数時間後に解消します。
背中の痛みや筋肉の痛みは、お薬を服用してから12〜24時間後に発生することがあり、これらの症状は通常、発症から48時間以内に解消します。
副作用がしばらく経っても治まらない場合は、医療機関に相談してください。
タダラフィルの副作用についてより詳しい情報を知りたい方はこちらをクリックして シアリスの副作用の記事をご参照ください。
タダラフィルを服用する前に、アレルギーがあるかどうかを医師または薬剤師に伝えてください。タダラフィルが含まれる医薬品には、アレルギー反応やその他の症状を引き起こす可能性のある不活性成分が含まれている場合があります。詳細については、医師に相談してください。
以下の病歴がある方、現在の病状を有する方は、タダラフィルを使用する前に、医師または薬剤師に必ず相談してください:
・心臓の疾患(過去6か月の心臓発作または生命を脅かす不規則な心拍、胸痛/狭心症、心不全など)
・脳卒中(過去6ヶ月)
・腎臓病
・肝臓病
・高血圧
・低血圧
・脱水症
・陰茎の疾患(湾曲症、線維症、ペロニー病など)
・持続勃起症(痛みを伴う長期にわたる勃起の症状)
・持続勃起症を引き起こす可能性のある病歴のある方(鎌状赤血球貧血、白血病、多発性骨髄腫など)
・眼の疾患(網膜色素変性症、突然の視力低下、NAIONなど)
・出血障害
・胃潰瘍
以上の病歴のある方は副作用が発症するリスクを高める可能性があります。
2005年5月、FDA(米国食品医薬品局)はタダラフィルと他のPDE5阻害薬がNAION(非動脈炎性前部虚血性視神経症)に関連する視力障害を引き起こすことがあることを発見しました。NAIONの患者のほとんどがPDE5の使用において解剖学的に、そして血管の危険因子があることがわかりました。 このことから、FDAは3つのPDE5阻害剤すべての説明書において、NAIONを有する患者のPDE5阻害薬の使用を注意するための変更を行いました。
2007年10月、FDAはタダラフィルを含むすべてのPDE5阻害薬において、PDE5阻害薬の使用に関連して一時的な難聴が一部の患者から報告されたとして、突然の聴力損失の潜在的リスクを勧告し、注意が促されました。
薬物の相互作用により、薬の作用が変化したり、深刻な副作用を引き起こすリスクが増加する場合があります。
タダラフィルと相互作用する可能性のある製品は、経口肺高血圧症治療薬であるリオシグアト(商品名:アデムパス)です。
タダラフィルは、ニトログリセリン、イソソルビド、亜硝酸アミルなど、胸痛や狭心症の治療に使用される硝酸薬と併用すると血圧が大幅に低下する可能性があり、めまい、失神、まれに心臓発作や脳卒中を引き起こす可能性があります。
– アルファ遮断薬(α遮断薬)
前立腺肥大症(BPH)や高血圧の治療薬であるドキサゾシン、タムスロシン塩酸塩などのアルファ遮断薬(α遮断薬)を服用している場合、血圧が下がりすぎてめまいや失神を引き起こす可能性があります。
医師は、タダラフィルを低用量で投与を開始するか、低血圧のリスクを最小限に抑えるためにアルファ遮断薬の用量を調整することがあります。
– タダラフィルの代謝に影響を与える医薬品
以下のお薬は身体からタダラフィルが代謝される作用に影響を与える可能性があり、タダラフィルの働きに影響を与える可能性があります。
上記のリストには、すべての薬物相互作用が含まれているわけではありません。使用するすべてのお薬、医薬品、ハーブ薬品、漢方薬、サプリメントなどのリストを医師と薬剤師に提示してください。
医師の承認なしに、お薬の投与を開始したり、停止したり、または用量を変更しないでください。服用する前に医師の診断を受け、医師の指定した用量や用法の指示に従い服用するようにしてください。
アメリカでは、1997年にFDAが処方薬のマーケティングに関する規則を緩和し、消費者を直接ターゲットにした広告を許可しました。アイコスとイーライリリーのジョイント・ベンチャー企業であるリリー・アイコス(Lilly-ICOS)は、ニューヨークのGrey Worldwide Agencyを雇用しシアリスの広告キャンペーンを実施しました。シアリスのマーケティング担当者は、他社と競合してお薬の広告の期間をより長く設定し、バイアグラなどのED治療薬とは異なる印象をテレビのコマーシャルで与えることに成功しました。
アメリカでのシアリスの広告では中高年のカップルが2つのバスタブを横に並べ、それぞれがバスタブに入りながら手をつなぎ、様々な自然の風景を眺めてくつろぐ様子が映し出され、話題となりました。カップルはビーチで海を、山頂からの景色を、湖の上からの景色などを仲睦まじく見ている様子が描かれました。
シアリスの初めてのCMは、2003年のスーパーボウルの放映時に登場し、バスタブにつかりながらくつろぐ夫婦の映像は、すぐにこのブランドの有名なシンボルになりました。長年にわたり、Cialisのバスタブ・カップルは進化し続け、新しい場所とさまざまなシチュエーションで紹介されました。シアリスのマーケティング担当のデブ・フセイン氏によると、浴槽はシアリスの長い効果持続時間を象徴的に表現しているそうです。シアリスの効果は最大36時間まで持続するので、男性に性交するタイミングの自由がより与えられ、心配せずにリラックスすることができるからです。
シアリスは2011年に良性前立腺肥大症(BPH)の治療へもFDAから承認を受けたので、2012年にはBPHへの適応が広告にも追加されました。
2014年までのシアリスの累積売上高は150億ドルを超え、2014年の売上高は23億ドルで、これまでで最大の売上高でした。
ニールセン・データによると、シアリスは2014年に最も宣伝された処方薬ブランドであり、実に2億4900万ドルもの広告費が費やされました。ED治療薬として競争相手であるバイアグラも大きな支出があり、2014年の支出では4位にランクされ、2億1,100万ドルが費やされました。
イーライリリー社にとって、バスタブのカップルの象徴的なマーケティングは成功し、大きな成果を上げました。
・アメリカのTIME誌は2003年のベスト発明のリストにシアリスを挙げました。
・シアリスは、2005年に「ブロックバスター・ステータス」を取得し、この時点で世界の売上高が10億ドルに達しました。
・2008年に、シアリスはアメリカで1日1回の使用が承認され、男性にEDを治療するための2つの異なる投与オプションを与えました。
・2011年、シアリスは、勃起不全(ED)と良性前立腺肥大症(BPH)の症状の両方を治療するための承認がFDAから降りた最初で唯一の医薬品となりました。
・2013年の10年間のレポートの時点までに、シアリスは世界中で推定4100万人の患者を治療しました。現在までにはより多くの男性たちがシアリスを服用していると推定することができます。
・シアリスは、泌尿器科医が最も処方する経口ED治療薬のうちの一つです。
シアリスの独占特許権は2017年11月に満了し、アメリカとイギリスなどの国々ではシアリスのジェネリック医薬品であるタダラフィル錠が販売されはじめました。
日本では2019年現在シアリスのジェネリック医薬品は承認されていません。日本国内のクリニックや病院でタダラフィル錠を入手することはできません。
日本国内からは、個人輸入代行サービスの通販を利用すると、シアリスのジェネリック医薬品であるタダラフィル錠を購入することができます。
シアリス ジェネリックを購入する方法についてより詳しい情報を知りたい方はこちらをクリックして シアリス ジェネリックの購入方法の記事をご参照ください。
タダラフィルは、イギリスの製薬会社であるグラクソウェルカム(現在のグラクソスミスクライン)とアメリカのバイオテクノロジー会社であるアイコス社(ICOS)のパートナーシップの下で発見され、1991年8月から新薬の開発が開始されました。当時、タダラフィルはIC351という化合物の名称で呼ばれていました。
1993年、アイコス社はホスホジエステラーゼ5型(PDE5)酵素の阻害剤である化合物IC351の研究を開始しました。
1994年、ファイザーの科学者はPDE5酵素を阻害するシルデナフィルが、心臓治療薬の臨床研究に参加している男性の報告により、陰茎の勃起を引き起こす効果があることを発見しました。 同年にアイコス社は化合物IC351の特許を取得し、1995年にフェーズ1臨床試験を開始しました。1997年にはED(勃起不全)を患う男性を対象にフェーズ2臨床試験を開始し、フェーズ3に進みました。
グラクソスミスクラインは当初、アイコス社と医薬品の利益を50%ずつ分け合うことで合意していましたが、開発された医薬品が同社の中核市場になかったため、グラクソスミスクラインは1996年に契約を失効させました。
1998年、アイコス社とイーライリリー社(Eli Lilly and Company)の合弁会社であるリリー・アイコス(Lilly ICOS)合同会社が設立され、ED治療薬として開発され始めました。
2000年にリリー・アイコスは、化合物IC351の新薬申請をFDAに提出しました。
2002年5月、リリー・アイコスは、アメリカの泌尿器科学会に、臨床試験でタダラフィルが最大36時間の有効性を示したことを報告し、1年後の2003年にFDAはタダラフィルをED治療薬として承認し、シアリスが国際的に販売され始めました。
日本では厚生労働省への申請が2005年9月に提出され、2007年に承認が降り、日本イーライリリー社からシアリスが販売されました。
2007年、アメリカのイーライリリー社はアイコス社を23億ドルで買収しました。その結果、イーライリリー社はシアリスの独占販売権を所有することになりました。
2009年にタダラフィルは、アメリカと日本などの国々で肺動脈性高血圧症(PAH)の治療薬として承認され、アドシルカ(Adcirca)として販売されました。
2009年7月より日本での発売元は日本新薬へ移され、日本イーライリリー社が製造販売、日本新薬が販売を行うことになりました。
2011年10月6日、FDAは、タダラフィルを良性前立腺過形成(BPH)の兆候と症状を治療するための治療薬としてシアリスを承認しました。
日本では、2014年に厚生労働省より承認され、「ザルティア」という商品名で販売が開始されました。
より詳しい情報を知りたい方はこちらをクリックして シアリスの歴史の記事をご参照ください。